La teoría cinética de los gases es una teoría física que explica el comportamiento y propiedades
macroscópicas de los gases a partir de una descripción estadística de los procesos moleculares
microscópicos. La teoría cinética se desarrolló con base en los estudios de físicos como
Ludwig Boltzmann y James Clerk Maxwell a finales del siglo XIX.
Principios
Los principios fundamentales de la teoría cinética son los siguientes:
- El número de moléculas es grande y la separación media entre ellas es grande comparada con sus
dimensiones. Por lo tanto ocupan un volumen despreciable en comparación con el volumen del envase
y se consideran masas puntuales.
- Las moléculas obedecen las leyes de Newton, pero individualmente se mueven en forma aleatoria
con diferentes velocidades cada una, pero con una velocidad promedio que no cambia con el tiempo.
- Las moléculas realizan choques elásticos entre sí, por lo tanto se conserva tanto el momento lineal
como la energía cinética de las moléculas.
- Las fuerzas entre moléculas son despreciables, excepto durante el choque. Se considera
que las fuerzas eléctricas o nucleares entre las moléculas son de corto alcance,
por lo tanto solo se consideran las fuerzas impulsivas que surgen durante el choque.
- El gas es considerado puro, es decir todas las moléculas son idénticas.
- El gas se encuentra en equilibrio térmico con las paredes del envase.
Estos postulados describen el comportamiento de un gas ideal. Los gases reales se aproximan a este
comportamiento ideal en condiciones de baja densidad y temperatura.
PRESIÓN
En el marco de la teoría cinética la presión de un gas es explicada como el resultado macroscópico
de las fuerzas implicadas por las colisiones de las moléculas del gas con las paredes del
contenedor. La presión puede definirse por lo tanto haciendo referencia a las propiedades microscópicas
del gas.
En general se cree que hay más presión si las partículas se encuentran en estado sólido, si se
encuentran en estado líquido es mínima la distancia entre una y otra y por último si se encuentra en
estado gaseoso se encuentran muy distantes.
En efecto, para un gas ideal con N moléculas, cada una de masa m y moviéndose con una velocidad
aleatoria promedio vrms contenido en un volumen cúbico V las partículas del gas impactan con
las paredes del recipiente de una manera que puede calcularse de manera estadística
intercambiando momento lineal con las paredes en cada choque y efectuando una fuerza neta
por unidad de área que es la presión ejercida por el gas sobre la superficie sólida.
La presión puede calcularse como:
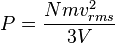 (gas ideal)
(gas ideal)Este resultado es interesante y significativo no sólo por ofrecer una forma de calcular la presión de un
gas sino porque relaciona una variable macroscópica observable, la presión, con la energía
cinética promedio por molécula, 1/2 mvrms², que es una magnitud microscópica no observable directamente.
Nótese que el producto de la presión por el volumen del recipiente es dos tercios de la energía cinética total
de las moléculas de gas contenidas.
TEMPERATURA
cinética molecular. La ley de los gases ideales nos permite asegurar que la presión es proporcional a la
temperatura absoluta. Estos dos enunciados permiten realizar una de las afirmaciones más importantes
de la teoría cinética: La energía molecular promedio es proporcional a la temperatura. La
constante de proporcionales es 3/2 la constante de Boltzmann, que a su vez es el cociente
entre la constante de los gases R entre el número de Avogadro. Este resultado permite deducir el
principio o teorema de equipartición de la energía.
La energía cinética por Kelvin es:
- Por mol 12,47 J
- Por molécula 20,7 yJ = 129 μeV
En condiciones estándar de presión y temperatura (273,15 K) se obtiene que la energía cinética
total del gas es:
- Por mol 3406 J
- Por molécula 5,65 zJ = 35,2 meV
Ejemplos:
- Dihidrógeno (peso molecular = 2): 1703 kJ/kg
- Dinitrógeno (peso molecular = 28): 122 kJ/kg
- Dioxígeno (peso molecular = 32): 106 kJ/kg
No hay comentarios:
Publicar un comentario